Перейти к:
ДИССОЦИАЦИЯ КЛИНИЧЕСКИХ ПРОЯВЛЕНИЙ И НЕЙРОВИЗУАЛИЗАЦИИ ПРИ ПРОГРЕССИРУЮЩЕМ НАДЪЯДЕРНОМ ПАРАЛИЧЕ (ПАРНОЕ КЛИНИЧЕСКОЕ НАБЛЮДЕНИЕ СИНДРОМА СТИЛА-РИЧАРДСОНА-ОЛЬШЕВСКОГО)
https://doi.org/10.57256/2949-0715-2025-4-4-83-92
Аннотация
Актуальность. Дифференциальная диагностика болезней двигательного нейрона представляется в практической врачебной деятельности весьма затруднительной. Особое значение имеет ранняя диагностика этой группы заболеваний, в частности, прогрессирующего надъядерного паралича. Патогномоничные клинические признаки и нейровизуализационные корреляты приобретают в данном случае решающее значение в верификации диагноза.
Описание клинических случаев. Представлены парные клинические наблюдения прогрессирующего надъядерного паралича, отличающиеся по признакам при проведении магнитно-резонансной томографии головного мозга. В статье описаны клинические наблюдения двух пациенток с прогрессирующим надъядерным параличом (синдромом Стила-Ричардсона-Ольшевского). Представлена детальная клиническая характеристика каждого случая. В первом случае получены характерные симптомы «колибри» и «Микки-Мауса». Во втором случае этих признаков не обнаружено. Обе пациентки находятся под наблюдением в клинике, что позволяет оперативно оценивать динамику клинического неврологического статуса, результаты лечения и проводить профилактическую работу по предупреждению опасных осложнений заболевания (дисфагия, падения). В обсуждении представлен дифференциальный ряд при прогрессирующем надъядерном параличе и возможности количественной автоматизированной и ручной планиметрии при анализе изображений магнитно-резонансной томографии головного мозга.
Заключение. Указанные подходы к ведению пациентов с прогрессирующим надъядерным параличом способствуют ранней диагностике заболевания, коррекции лечения, профилактике осложнений.
Ключевые слова
Для цитирования:
Быков Ю.Н., Панферова Е.И., Загвозкина Т.Н., Скворцова Ю.А., Широкова А.В. ДИССОЦИАЦИЯ КЛИНИЧЕСКИХ ПРОЯВЛЕНИЙ И НЕЙРОВИЗУАЛИЗАЦИИ ПРИ ПРОГРЕССИРУЮЩЕМ НАДЪЯДЕРНОМ ПАРАЛИЧЕ (ПАРНОЕ КЛИНИЧЕСКОЕ НАБЛЮДЕНИЕ СИНДРОМА СТИЛА-РИЧАРДСОНА-ОЛЬШЕВСКОГО). Байкальский медицинский журнал. 2025;4(4):83-92. https://doi.org/10.57256/2949-0715-2025-4-4-83-92
For citation:
Bykov Yu., Panferova E., Zagvozkina T., Skvortsova I., Shirokova A. DISSOCIATION OF CLINICAL MANIFESTATIONS AND NEUROIMAGING IN PROGRESSIVE SUPRANUCLEAR PALSY (PAIRED CLINICAL CASE OF STEELE-RICHARDSON-OLSHEVSKY SYNDROME). Baikal Medical Journal. 2025;4(4):83-92. (In Russ.) https://doi.org/10.57256/2949-0715-2025-4-4-83-92
Введение
Прогрессирующий надъядерный паралич (ПНП) – клинически гетерогенное, нейродегенеративное заболевание из группы таупатий, описанное Стилом, Ричардсоном и Ольшевским в середине XX века. Заболевание характеризуется ранним развитием постуральной неустойчивости (с преимущественным падением назад), парезом вертикального взора (в том числе с блефароспазмом, акинезией век, замедленностью произвольных движений глаз), различными сочетаниями атипичного паркинсонизма (с аксиальной ригидностью, симметричностью, минимальным или отсутствующим ответом на L-DOPA) и когнитивными дисфункциями подкорково-лобного типа (в виде импульсивности, бестактности, проблем с планированием и принятием решений). ПНП составляет около 5,5 % всех случаев паркинсонизма, считаясь второй по частоте формой нейродегенеративного паркинсонизма [1, 2]. Согласно эпидемиологическим данным, полученным в ходе различных популяционных исследований, распространенность ПНП составляет 5–6 случаев на 100 тыс. населения, а дебют заболевания приходится на шестое – седьмое десятилетие жизни [1, 3, 4].
ПНП связан со спорадической аномалией белка тау, вызывающей его гиперфосфорилирование с последующей агрегацией с образованием нейрофибриллярных клубков, что приводит к развитию нейродегенерации. При ПНП дегенерация характеризуется преимущественно региональной атрофией среднего мозга, однако структурная трансформация может включать такие области, как бледный шар, субталамические ядра, ножки мозга, таламус, область верхних мозжечковых ножек, в меньшей степени - лобная и височная кора [5, 6]. Развитие клинической картины зависит от порядка вовлечения в патологический процесс указанных структур, а также от степени их дегенерации. Классическая картина ПНП встречается у большинства пациентов, однако, ПНП может проявляться широким фенотипическим спектром, пересекающимся с другими нейродегенеративными расстройствами, что может затруднять раннюю и верифицированную диагностику.
ПНП относится к группе заболеваний «паркинсонизм +», сочетая в себе не только признаки паркинсонизма, но и признаки, отражающие поражение других участков центральной нервной системы. Критерии Национального института неврологических расстройств и инсульта и Общества прогрессирующего надъядерного паралича (NINDS-SPSP, 1996) активно использовались для диагностики случаев классического ПНП Стила-Ричардсона-Ольшевского. Они базировались на прогрессирующем течении заболевания с дебютом после 40 лет, наличии пареза вертикального взора и развития постуральной неустойчивости с частыми падениями с момента возникновения первых симптомов при исключении других причин, обуславливающих развитие подобной симптоматики (в том числе васкулярный паркинсонизм и нормотензивная гидроцефалия). При этом учитывались "красные флаги" других заболеваний: галлюцинации, перенесенный энцефалит, автономная дисфункция, когнитивные флюктуации [7]. Публикация новых результатов исследований в области нейродегенеративных заболеваний принесла новые знания о различиях в клинических проявлениях ПНП, что усложнило использование традиционных клинических критериев для своевременного и точного определения различных фенотипов заболевания [6, 8]. Многочисленные комбинации создают гетерогенность заболевания, объединяя в себе множество фенотипов, варианты которого были недавно проанализированы и сгруппированы в обновленных критериях общества двигательных расстройств (MDS, 2017), что обеспечивает возможность диагностики полного диапазона ПНП-подтипов [9]. Несмотря на специфичность критериев, достоверный диагноз ПНП выставляется только на основании посмертного гистопатологического исследования.
Поскольку в основе заболевания лежит нейродегенеративный процесс, то постепенное вовлечение все новых участков головного мозга с последующей деструкцией приводит к уменьшению площади нервной ткани, фиксируемой методами нейровизуализации. Признаки, полученные при использовании различных методов визуализации в рамках данной клинически гетерогенной группы, рассматриваются как дополнительный инструмент и не используются для постановки окончательного диагноза. Общие признаки при магнитно-резонансной томографии (МРТ) ПНП включают диспропорциональную атрофию дорсальной части среднего мозга (симптом «колибри», симптом «Микки-Мауса»), изменения архитектуры верхних мозжечковых ножек, фронтальную корковую атрофию, расширение пространств третьего желудочка и области водопровода [5, 6, 10]. Согласно результатам нескольких исследований, использование традиционного визуального анализа МРТ-изображений является специфичным, но менее чувствительным, чем клиническая диагностика [10].
Однако, чувствительность МРТ-признаков ограничена (медиана 24 %) при первых сеансах нейровизуализаций [10]. Диагноз обычно ставится через несколько лет после появления первых симптомов, когда ключевые признаки достигают своего полного проявления [9]. Тем не менее, ценность данных, полученных при анализе изображений МРТ, остается недостаточно понятной, особенно в отношении многочисленных фенотипов ПНП и состояний по типу overlap.
Клиническое наблюдение 1
Пациентка Ж., 61 год, в сентябре 2025 года была госпитализирована в клинику нервных болезней Иркутского государственного медицинского университета для уточнения диагноза и назначения симптоматического лечения с направительным диагнозом: «Прогрессирующая надъядерная офтальмоплегия Стила-Ричардсона-Ольшевского».
Жалобы при поступлении: на нарушение координации движений и «шаткость» походки, иногда возникающие падения (больше назад), нарушение мочеиспускания (недержание мочи), нарушение сна (трудности засыпания), периодический шум в ушах, повышенную тревожность, необоснованный ситуацией плач, изменение почерка.
Считает себя больной в течение 2 лет, когда впервые стала отмечать падения при передвижениях, с большей направленностью назад. В течение года от момента возникновения указанных жалоб за медицинской помощью не обращалась, лечение не получала. Состояние оставалось стабильным, без значимых ухудшений, для передвижения пользовалась тростью. Со слов супруга в указанные период времени окружающие стали замечать изменение характера пациентки (повышенная тревожность, «бессвязность» речи, некоторая импульсивность). У пациентки не наблюдалось сопутствующего тремора, непроизвольного устойчивого положения конечности или шеи, подергивания конечностей, зрительных галлюцинаций, дисфагии или двигательной слабости. Дальнейшее интервьюирование показало, что симптомы постепенно ухудшались в течение года.
Впервые обратилась к неврологу по месту жительства в ноябре 2024 года. Выставлен диагноз: «Хроническая ишемия головного мозга, 2 степени, Атеросклероз церебральных сосудов. Выраженный вестибулоатактический синдром. Элементы дизартрии». После первого обращения выполнены исследования в виде общего клинического минимума, а также дополнительные методы согласно сопутствующей патологии, в том числе МРТ головного мозга и ультразвукового исследования (УЗИ) брахио-цефальных артерий (БЦА).
Результаты МРТ головного мозга от ноября 2024 года (Рис. 1): «МР-признаки нейродегенеративного процесса с преимущественным поражением среднего мозга (средний мозг уменьшен в объёме, соотношение «средний мозг-мост» уменьшено до 0,18 (референс от 0,24), симптомы «колибри» и «Микки-Мауса» (возможный прогрессирующий надъядерный паралич). Очаговые изменения белого вещества мозга сосудистого характера категории Fazekas 1. Глобальная корковая атрофия (GCA) 1 степени. Признаки внутричерепной гипертензии, либо исхода внутричерепной гипертензии (коррелировать с клиническими проявлениями)». УЗИ БЦА от ноября 2024 года: «Признаки начального атеросклероза БЦА в виде увеличения толщины комплекса интима-медиа (ТИМ) в каротидной бифуркации справа. Волнообразная деформация правой внутренней сонной артерии (ВСА) и С-образная деформация правой позвоночной артерии (ПА) в VI сегменте без локальных нарушений кровотока. Гипоплазия правой левой ПА. Снижение скоростных показателей кровотока по левой ПА в V1-2 сегментах».
В январе 2025 года проведена повторная консультация невролога. На основании данных жалоб, анамнеза, осмотра, данных дополнительных обследований выставлен следующий предположительный диагноз: «Прогрессирующий надъядерный паралич. Умеренно выраженный акинетико-ригидный синдром. Умеренная постуральная неустойчивость. Умеренные глазодвигательные нарушения (парез вертикального взора). Нерезко выраженный псевдобульбарный синдром. Умеренные вегетативные нарушения (нарушения функции тазовых органов по типу недержание мочи)». Рекомендовано: Tab. Levodopa 250+Carbidopae 25 mg (ТИДОМЕТ-ФОРТЕ 250 мг) 1/4 табл. с постепенным нарастанием дозировки с 12 недели до 1/2 табл. утром, 1 табл. в обед, 1 табл. вечером, Tab. Amantadini sulfitis 0,1 (ПК-МЕРЦ 100 мг) 1/2 табл. утром, с постепенным повышением дозировки и кратности с 4 недели до 1 табл. 2 раза в день.
В марте 2025 была проведена повторная консультация невролога по месту жительства для оценки динамики развития заболевания и корректировки лечения. Были даны следующие рекомендации: Tab. Levodopa 250+Carbidopae 25 mg (ТИДОМЕТ-ФОРТЕ 250 мг) 1/2 табл. 4 раза в день, Tab. Amantadini sulfatis 0,1 (ПК-МЕРЦ 100 мг): 1,5 табл. 2 раза в день. В июле 2025 года была проведена очередная консультация невролога – проведена коррекция терапии Таb. Levodopac 250+Carbidopac 25 mg (ТИДОМЕТ-ФОРТЕ 250 мг) 1/2 табл. 3 раза в день (утро, обед, вечер), 3/4 табл. на ночь 3 недели, затем по 1/2 табл. 3 раза в день (утро, обед, вечер), 1 табл. на ночь. Tab. Amantadini sulfatis 0,1 (ПК-МЕРЦ 100 мг): 1,5 табл. 2 раза в день.
Изменения своего состояния на протяжении всего периода применения указанных схем лечения и дозировок не отмечалось. Направлена и госпитализирована в неврологическое отделение клиник Иркутского государственного медицинского университета для уточнения диагноза и определении дальнейшей тактики ведения.
При осмотре в клинике: температура — 36,50С, рост — 164 см, вес — 74 кг. Индекс массы тела — 27,51 кг/м2. Состояние пациентки удовлетворительное. Сознание ясное. Положение больной активное; астеник. Выявляется грудопоясничный кифосколиоз.
В неврологическом статусе выявлены следующие изменения: движение глазных яблок несколько ограничены при взгляде влево и вверх, произвольные движения глаз по вертикали замедленны. Зрачковые реакции на свет снижены. Зрачковые реакции на конвергенцию отсутствуют. Зрачковые реакции на аккомодацию отсутствуют. «Удивленное выражение лица», вертикальные морщины на лбу (Procerus sign). Блуждающие движения глазных яблок при попытке взгляда вверх (описываемый в литературе симптом «round-the-house saccade»), дисфиксационные саккады. Дисфагия. Дужки мягкого неба стоят низко, при фонации подвижны. Глоточный рефлекс отсутствует. Язык отклонен влево. Рефлексы орального автоматизма: ладонно-подбородочный рефлекс Маринеску-Радовичи с обеих сторон. Тонус мышц: в руках гипотония, в ногах гипотония. Гипертонус верхней осевой аксиальной мускулатуры. Ретроколлис. Карпорадиальные высокие: S>D. С бицепса высокие: S>D. С трицепса высокие: S>D. Коленные рефлексы высокие: S>D. Ахилловы рефлексы высокие: S>D. Патологические рефлексы: верхний рефлекс Россолимо слева. Походка широкая (Gunslinger sign), передвигается с тростью. Подавление вестибулоокулярного рефлекса сохранено.
На основании жалоб, анамнеза, данных осмотра и результатах дополнительных методов исследований выставлен окончательный диагноз: «Прогрессирующий надъядерный паралич. Нерезко выраженный псевдобульбарный синдром. Умеренные вегетативные нарушения (по типу недержания мочи)». Сопутствующий диагноз: «Гипертоническая болезнь, достигнуто целевое давление II стадии, риск 3 (нарушение гликемии натощак, окружность талии более 88 см, общий холестерин более 4.9 ммоль/л, холестерин липопротеидов низкой плотности более 3,0 ммоль/л). Нарушение гликемии натощак. Избыточная масса тела. Дислипидемия 2А. Желче-каменная болезнь. Хронический калькулезный холецистит, ремиссия. Хронический билиарнозависимый панкреатит без нарушения функции поджелудочной железы, болевая форма, редко рецидивирующее течение, ремиссия. Хронический цистит, латентное течение. Неполная осложненная катаракта, Миопия средней степени, Гипертоническая ангиопатия сетчатки обоих глаз».
Проведенное лечение: 1) раствор холина альфосцерат 250 мг/мл - 4 мл + р-р натрия хлорид 0,9 % - 250 мл в/в капельно - 1 раз в день; 2) раствор этилметилгидроксипиридина сукцинат 50 мг/мл - 4 мл в/м 1 раз в день; 3) лиофилизированный ницерголин 4 мг в/м 1 раз в день; 4) табл. ПК-Мерц 150 мг перорально 2 раза в день до 18.09.2025; 5) р-р ПК- Мерц 500,0 мл в/в капельно № 5 с 19.09.2025; 6) табл. леводопа-карбидопа (250 мг+ 25 мг), 0.5 табл перорально - 3 раза в день (утро, день, вечер), 1 таблетка на ночь; гипотензивная терапия; курс лечебной физкультуры и физиолечение.
Рекомендовано: Наблюдение у невролога, повторная госпитализация через 6 месяцев в неврологическое отделение клиник Иркутского государственного медицинского университета. Создание безопасной среды (использование поручней, ходунков, трости), модификация диеты для предотвращения аспирации, использование искусственных загустителей пищи. МРТ головного мозга по программе нейродегенеративных заболеваний (с акцентом на изменения в среднем мозге). Рекомендовано проведение протонной магнитно-резонансной спектроскопии (ПМРС) с определением уровня N-ацетиласпартата в проекции скорлупы в плановом порядке. В связи с недержанием мочи пациентке рекомендовано прохождение УЗИ мочевого пузыря с оценкой остаточной мочи с последующей консультацией уролога. Продолжить прием амбулаторно курсом: 1) капс. холина альфосцерат 400 мг 2 раза в день 2 месяца, табл.; 2) ПК- Мерц 150 мг перорально 2 раза в день, коррекция дозы по потребности; 3) табл. леводопа-карбидопа (250 мг + 25 мг) 1 табл., перорально 1 раз в день в 23.00 1/2 табл. 3 раза в день.
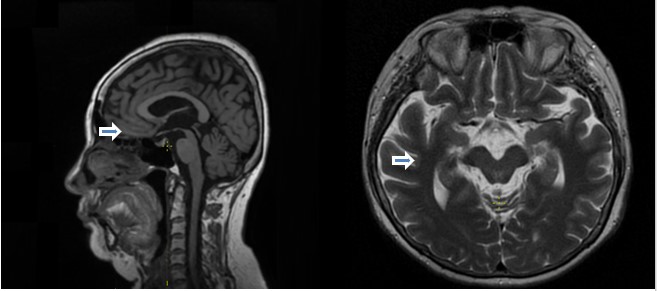
Рис. 1. Регистрация симптома «колибри» и «Мики-Мауса» (указано стрелкой) на МРТ-изображении головного мозга в сагиттальных и аксиальных проекциях, больная Ж., 61 год.
Fig. 1. Registration of «hummingbird» and «Mickey Mouse» signs on the MRI image in sagittal and axial projections, patient G., 61 years old.
Клиническое наблюдение 2
Пациентка М, 52 года, обратилась в клинику нервных болезней Иркутского государственного медицинского университета для уточнения диагноза. При поступлении пациентка жаловалась на несистемные головокружения, неустойчивость, «шаткость» при ходьбе с падениями назад, трудности с засыпанием, замедление речи, снижение зрения с появлением черно-белых пятен перед взором по утрам при переходе в вертикальное положение, размытое и нечеткое зрение в течение дня, сильную потливость по ночам, появление храпа.
Жалобы появились в 2023 году, когда впервые пациентка стала замечать несистемное головокружение и, как следствие, неустойчивость при ходьбе. Коллеги по работе отметили появление шепелявости, однако сама пациентка не замечала за собой нарушений речи. По ночам появился храп. Пациентка лечилась по месту жительства в терапевтическом стационаре, где проходила лечение следующими препаратами: р-р цитиколина внутривенно капельно, р-р этилметилгидроксипиридина сукцинат внутривенно, таб. глицин и таб. бетагистин. Пациентка не отметила какого-либо эффекта. В апреле 2024 года появилось резкое ухудшение речи с невозможностью выговаривать слова в течение суток, за экстренной медицинской помощью не обратилась, после спонтанного улучшения самостоятельно выполнила МРТ-исследование головного мозга, где выявлены монофокальные глиозные изменения белого вещества головного мозга, неспецифического (дисциркуляторного?) генеза. После консультации невролога по месту жительства выставлен диагноз: «Вестибуло-атакический синдром, дифференциальная диагностика с дисциркуляторной энцефалопатией цервикогенного генеза, демиелинизирующим заболеванием, соматоформной дисфункцией на фоне тревожно-депрессивного расстройства». Назначено лечение: р-р депротеинизированный гемодериват крови крупного рогатого скота (актовегин) внутривенно, таб. экстракт Гинкго билоба (танакан) 40 мг, таб. буспирон (веспирейт) 15 мг и таб. пароксетин 20 мг в течение месяца, однако без эффекта. В августе 2024 г. снова проведен курс лечения - р-р инозин+никотинамид+рибофлавин+янтарная кислота (цитофлавин) в/в, р-р этилметилгидроксипиридина сукцинат (мексидол) в/в, таб. бетагистин и вновь без эффекта. Консультирована неврологом консультативно-диагностической поликлиники Иркутской областной клинической больницы от 04.09.2024 г., Заключение: «Вегетативно-сосудистая дистония, тревожно-депрессивный синдром с диссомнией». На момент осмотра вестибуло-координаторных и атактический нарушений не выявлено». Психолог от 04.09.2024 г.: «Снижение эмоционально-волевой сферы (тревожно-депрессивный фон)». В течение последующего года самочувствие ухудшилось, симптомы постепенно усиливались. Тест МОСА (амбулаторно): 19 баллов из 30. При УЗИ щитовидной железы от 08.04.24 г.: «Узел правой доли - TRADS 2». Гормоны щитовидной железы в пределах нормы. УЗИ БЦА от 22.04.24 г.: «Атеросклероз сонных артерий с локальным стенозом в бифуркации справа 25 %, слева 20 %». Консультация офтальмолога 13.09.24 г.: «Гиперметропия слабой степени тяжести, пресбиопия обоих глаз». МРТ головного мозга по протоколу диагностики нейродегенеративных заболеваний от 16.12.2024 г. (Рисунок 2): «Структурных изменений головного мозга, избирательной гиппокампальной атрофии, данных за болезни Паркинсона и Альцгеймера не выявлено». Для уточнения диагноза направлена в неврологический стационар Иркутского государственного медицинского университета с 17.01.25 по 27.01.25 г. Выписана с диагнозом: «Нейродегенеративное заболевание с преимущественным вовлечением мозжечковых структур, зоны гиппокампа, надъядерных структур, мозжечковый синдром (атаксия, дисметрия, нистагм, дизартрия), элементы псевдобульбарного синдрома (положительные рефлексы орального автоматизма), умеренные когнитивные нарушения (шкала МОСА 18 баллов), элементы акинетико-ригидного синдрома (ахейрокинез, гипомимия, шаркающая походка), диссомнический синдром».
Однако за период с февраля по сентябрь 2025 года пациентка отмечает прогрессирующее ухудшение самочувствия, с появлением потливости, ухудшения зрения в виде черно-белых пятен перед взором по утрам, нарушение походки и речи. Анамнез жизни без особенностей, вредные привычки и хронические болезни отрицает. Постоянно принимает таб. карведилол 2,5 мг 2 р/сут, таб. аторвастатин 20 мг вечером, капс. церепро 3 р/сут.
Повторно госпитализирована в клинику нервных болезней Иркутского государственного медицинского университета в сентябре 2025 г.
При осмотре: температура - 36,00С, рост - 163 см, вес - 80 кг. Индекс массы тела - 30, 11 кг/м2. Состояние пациентки удовлетворительное. Сознание ясное, 15 б по Глазго. Положение больной активное, нормостеник. Артериальное давление 130/90 мм.рт.ст., ЧСС 66 ударов в минуту.
Во время осмотра в неврологическом статусе отмечены следующие отклонения: движения глазных яблок замедлены, в полном объёме, отмечается симптом Грефе, горизонтальный крупноразмашистый нистагм, Блуждающие движения глазных яблок при попытке взгляда вверх - окольный симптом ("round-the-house saccade"), девиация языка вправо, дизартрия, дисфония, замедленность речи, рефлексы орального автоматизма - ладонно-подбородочный рефлекс Маринеску-Радовичи с двух сторон, сосательный рефлекс, нижняя проба Барре - положительная справа, гипертонус по типу "складного ножа" в верхних конечностях, высокие карпорадиальные рефлексы, выявление патологических рефлексов Россолимо и Жуковского справа, гипотонус в нижних конечностях, походка с широко расставленными ногами (Gunslinger sign). В позе Ромберга устойчива, в усложненной падает назад. Гипергидроз не выявлен.
На основании жалоб, анамнеза, данных неврологического осмотра и дополнительных методов исследования выставлен окончательный диагноз: «Прогрессирующий надъядерный паралич. Акинетико-ригидный синдром с акцентом в проксимальных отделах. Ретропульсии. Парез взора (вверх и вниз). Элементы мозжечкового синдрома. Дизартрия. Двусторонняя пирамидная недостаточность. Сопутствующие заболевания: Пресбиопия обоих глаз».
В виду жалоб на сильную потливость по ночам и неустойчивость походки, проведена дифференциальная диагностика с мультисистемной атрофией (МСА). Дермаграфизм бледно-розовый, рефлекс гусиной кожи отрицательный, ортоклинопроба парадоксальная: частота сердечных сокращений и артериальное давление при переходе в вертикальное положение (пульс с 80 в минуту до 68 в минуту, АД от 100/60 мм.рт.ст. до 90/70 мм.рт.ст.), ускорение при возращении в горизонтальное положение (пульс с 68 в минуту до 74 в минуту, АД с 90/70 мм.рт.ст до 100/70 мм.рт.ст.), проба Даньини-Ашнера с симпатическим возбуждением (изменения частоты пульса не зарегистрировано). В данном случае характерных вегетативных изменений МСА не выявлено.
Проведенное лечение: р-р комплекс пептидов, полученных из головного мозга свиньи 10 мл + р-р натрия хлорид 0.9% 250 мл в/в капельно 1 раз утром, р-р этилметилгидроксипиридина сукцинат 50 мг/мл - 4 мл в/м 1 раз в день (утром), таб. бетагистин 24 мг перорально-2 раза в день (утро, вечер), таб. карведилол 12.5 мг перорально -2 раза в день (утро, вечер), с 18.09.25 по 25 мг перорально-2 раза в день (утро, вечер); таб. Ацетилсалициловая кислота 100 мг перорально - 1 раз в день (вечером); таб. пирибедил 50 мг перорально 2 раза в день (утром, вечером); таб. розувастатин 5 мг перорально 1 раз в день (вечером) с 16.09 по 21.09; таб. леводопа+карбидопа (250 мг+ 25 мг) 0,5 таб. перорально 2 раза в день (утро, вечер) с 19.09.2025, курс физиолечения. На фоне получаемых препаратов L-DOPA пациентка не отмечала заметных улучшений своего состояния.
Рекомендовано: наблюдение невролога, паркинсонолога, терапевта, офтальмолога по месту жительства, психиатра при необходимости, контроль липидограммы амбулаторно. Повторная госпитализация через 6 мес. в неврологическое отделение клиник Иркутского государственного медицинского университета для динамического контроля, решения вопроса проведения курса ПК-Мерц 500 в/в капельно в течение 5-7 дней. Создание безопасной среды (при неустойчивости и падениях - использование поручней, трости) при возникновении проблем с глотанием и приемом пищи - модификация диеты для предотвращения аспирации, использование искусственных загустителей пищи).
Продолжить амбулаторно прием: 1) капс. холина альфосцерат 400 мг - 2 р/сут (утром, в обед) 2 месяца; 2) таб. леводопа+карбидопа (250 мг + 25 мг) перорально по 1/2 табл. 3 раза в день с последующей коррекцией дозы неврологом при необходимости. Начать прием тaб. ПК-Мерц 100 мг 2 p/сут, c последующей коррекцией дозы неврологом при необходимости.
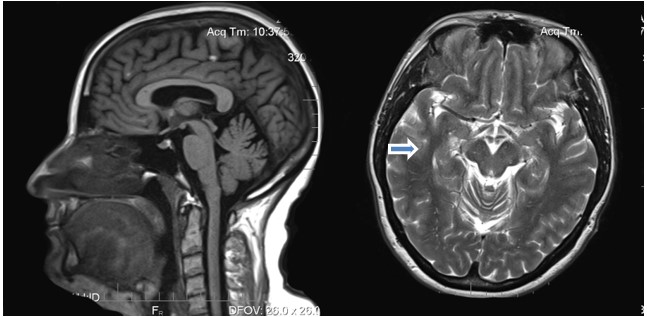
Рис 2. МРТ головного мозга пациентки М., 52 года. Возможный симптом «Мики-Мауса» (указано стрелкой авторами статьи).
Fig. 2. MRI of а 52- year-old female patient M. Possible "Mickey Mouse" symptom (indicated by arrow by the authors of the article).
Обсуждение
Классическая картина прогрессирующего надъядерного паралича (синдром Стила-Ричардсона-Ольшевского) встречается у большинства пациентов с данной нозологией [11, 12]. Однако ПНП может проявляться широким фенотипическим спектром, пересекающимся с другими нейродегенеративными расстройствами, в частности, мультисистемной атрофии, кортико-базальной дегенерации, что может затруднять раннюю и верифицированную диагностику ПНП.
Диагностика ПНП в основном базируется на основных клинических и ряда дополнительных признаках, которые включены в диагностические критерии Общества по изучению двигательных расстройств (MDS, 2017) [9, 13, 14].
Представленные клинические случаи демонстрируют сходство и различия в клинических проявлениях основного заболевания.
Сходства заключаются в развитии ранних симптомов с нарушения походки с преимущественным падением назад, длительности течения заболевания, изменении четкости речи, повышенной тревожности пациенток. В обоих случаях это женщины средних лет. Начало болезни проявилось в виде появления «шаткости» и неустойчивости походки, к которым со временем присоединялись ретропульсии. У обеих отмечались признаки паркинсонизма с недостаточной эффективностью при лечении препаратами леводопы. Кроме этого, за 2 года до дебюта болезни возник один из самых характерных для ПНП симптомов – парез вертикального взора [15]. Однако, это был не первый симптом в клинической картине.
При осмотре обращают на себя внимание объективные признаки глазодвигательных нарушений, изменение походки и неустойчивость пациенток в позе Ромберга. При УЗИ БЦА минимальные проявления атеросклероза без гемодинамически значимых стенозов, что исключает сосудистый генез клинических проявлений. Кроме этого, обе пациентки получали ноотропное, анксиолитическое лечение. Обе получали препараты леводопы, однако, отчетливого ответа на нее в обоих случаях не выявлено.
Клинические отличия заключаются в следующем. У пациентки Ж. имело место наличие тазовых нарушений по типу недержания мочи, психо-аффективные нарушения (повышенная тревожность, "бессвязность" речи, некоторая импульсивность, немотивированная плаксивость), признаки дисфагии (элементы псевдобульбарного синдрома). У пациентки М. наблюдались выраженные проявления вегетативных нарушений (потливость по ночам), когнитивные нарушения по данным опросника МоСА.
Наиболее ярким и существенным феноменом является диссоциация клинических проявлений с данными нейровизуализации. Две пациентки, примерно одного возраста, с приблизительно одной длительностью заболевания и степенью выраженности клинической картины демонстрируют разную степень поражения и вовлеченности структур головного мозга по данным МРТ диагностики: если в первом случае у пациентки с классической картиной ПНП обнаружены симптомы «Микки-Мауса» и «колибри», то во втором случае на фоне выраженной картины поражения головного мозга, МРТ изображения не демонстрируют характерных признаков.
Представленная клиническая картина надъядерного пареза вертикального взора (особенно, при взгляде вниз), ранних постуральных нарушений с падениями назад, псевдобульбарного синдрома, аксиальной ригидности в сочетании с характерными изменениями на МРТ (симптом "колибри", "Мики-Мауса") с высокой долей вероятности указывает на прогрессирующий надъядерный паралич (синдром Ричардсона) по критериям шкалы MDS (2017) для пациентки Ж.: О1+Р1, дополнительные критерии - А2, С2, СС2, IF1, для пациентки М.: О1+Р2, дополнительные критерии А2, С1-2, СС2. Недостаточная или отсутствующая эффективность ответа на терапию леводопой и неуклонное прогрессирование симптоматики подтверждает нейродегенеративную природу заболевания. Дальнейшая тактика должна быть направлена на симптоматическое лечение, реабилитацию и поддержку пациента и его семьи.
Серьёзной проблемой клинической диагностики ПНП является наличие подтипов заболевания и перекрестных состояний (overlap), клинические проявления которых совпадают с таковыми при других расстройствах паркинсонического спектра [16, 17].
Дифференциальный диагноз проводился со следующими нозологиями:
Мультисистемная атрофия (МСА): повышенное потоотделение, потемнение в глазах при резком переходе в вертикальное положение и изменения в ортоклинопробе у пациентки М. Отсутствие выраженной атаксии, наличие надъядерного пареза взора, падения на ранних стадиях развития заболевания позволили исключить данный диагноз [18].
Болезнь Паркинсона (БП): у обеих пациенток отмечается акинетико-ригидный синдром, гипомимия, однако при БП обычно имеется хороший и устойчивый ответ на препараты леводопы, в клинической картине на ранних стадиях преобладает тремор покоя, а не постуральная неустойчивость, нехарактерен надъядерный парез взора [19].
Сосудистая энцефалопатия (хроническая ишемия мозга): наличие атеросклероза ПА в обоих случаях на УЗИ БЦА, изменения по Fazekas 1 на МРТ [20]. Однако сосудистая энцефалопатия не объясняет весь комплекс симптомов, особенно специфические глазодвигательные нарушения и характерные для ПНП изменения среднего мозга. Отсутствие эффекта от многократных курсов сосудистой терапии также не дает возможности выставить этот диагноз.
Болезнь с тельцами Леви: когнитивные нарушения у пациентки М, диссомния у пациентки Ж. Однако отсутствие четких зрительных галлюцинаций и флюктуаций сознания при наличии надъядерного пареза взора исключает данный диагноз [21].
Заключение
Диссоциация между клинической картиной и данными нейровизуализации при прогрессирующем надъядерном параличе представляет собой важную проблему для диагностики и оценки заболевания. Нередко у пациентов клинические проявления заболевания существенно превосходят или не соответствуют видимым на МРТ изменениям. Эти различия могут объясняться ранней стадией развития заболевания, при которой структурные изменения еще не достигли уровня, визуально заметного на изображениях. Значительное расхождение между клиническими показателями и данными МРТ усложняет своевременную постановку диагноза и требует комплексного сопоставления клинических данных с результатами дополнительной диагностики для более точной оценки стадии и прогрессирования ПНП.
Список литературы
1. Arena J.E., Weigand S.D., Whitwell J.L. et al. Progressive supranuclear palsy: progression and survival. J Neurol. 2016;263(2):380-389. https://doi.org/10.1007/s00415-015-7990-2
2. Lim J., Malhotra A., Yong S.J. Atypical parkinsonism: Case-based learning on progressive supranuclear palsy. Aust J Gen Pract. 2022;51(12):967-969. https://doi.org/10.31128/AJGP-05-22-6413
3. Shoeibi A., Olfati N., Litvan I. Frontrunner in Translation: Progressive Supranuclear Palsy. Front Neurol. 2019;10:1125. https://doi.org/10.3389/fneur.2019.01125
4. Swallow D.M.A., Zheng C.S., Counsell C.E. Systematic Review of Prevalence Studies of Progressive Supranuclear Palsy and Corticobasal Syndrome. Mov Disord Clin Pract. 2022;9(5):604-613. https://doi.org/10.1002/mdc3.13489
5. Alster P., Kutyłowski M., Madetko-Alster N. Magnetic Resonance Imaging in the Neuroimaging of Progressive Supranuclear Palsy-Parkinsonism Predominant: Limitations and Strengths in Clinical Evaluation. Diagnostics (Basel). 2025;15(8):945. https://doi.org/10.3390/diagnostics15080945
6. Mahale R.R., Krishnan S., Divya K.P. et al. Subtypes of PSP and Prognosis: A Retrospective Analysis. Ann Indian Acad Neurol. 2021;24(1):56-62. https://doi.org/10.4103/aian.AIAN_611_20
7. Litvan I., Agid Y., Calne D. et al. Clinical research criteria for the diagnosis of progressive supranuclear palsy (Steele-Richardson-Olszewski syndrome): report of the NINDS-SPSP international workshop. Neurology. 1996;47(1):1-9. https://doi.org/10.1212/wnl.47.1.1
8. Nasri A., Sghaier I., Neji A. et al. Phenotypic Spectrum of Progressive Supranuclear Palsy: Clinical Study and Apolipoprotein E Effect. J Mov Disord. 2024;17(2):158-170. https://doi.org/10.14802/jmd.23178
9. Höglinger G.U., Respondek G., Stamelou M. et al. Clinical diagnosis of progressive supranuclear palsy: The movement disorder society criteria. Mov Disord. 2017;32(6):853-864. https://doi.org/10.1002/mds.26987
10. Anyfantakis G., Manouvelou S., Koutoulidis V. et al. Can Progressive Supranuclear Palsy Be Accurately Identified via MRI with the Use of Visual Rating Scales and Signs? Biomedicines. 2025;13(5):1009. https://doi.org/10.3390/biomedicines13051009
11. Ichikawa-Escamilla E., Velasco-Martínez R.A., Adalid-Peralta L. Progressive Supranuclear Palsy Syndrome: An Overview. IBRO Neurosci Rep. 2024;16:598-608. https://doi.org/10.1016/j.ibneur.2024.04.008
12. Madetko-Alster N., Otto-Ślusarczyk D., Wiercińska-Drapało A. et al. Clinical Phenotypes of Progressive Supranuclear Palsy-The Differences in Interleukin Patterns. Int J Mol Sci. 2023;24(20):15135. https://doi.org/10.3390/ijms242015135
13. Frank A., Peikert K., Linn J., Brandt M.D., Hermann A. MDS criteria for the diagnosis of progressive supranuclear palsy overemphasize Richardson syndrome. Ann Clin Transl Neurol. 2020;7(9):1702-1707. https://doi.org/10.1002/acn3.51065
14. Ali F., Martin P.R., Botha H. et al. Sensitivity and Specificity of Diagnostic Criteria for Progressive Supranuclear Palsy. Mov Disord. 2019;34(8):1144-1153. https://doi.org/10.1002/mds.27619
15. Giagkou N., Höglinger G.U., Stamelou M. Progressive supranuclear palsy. Int Rev Neurobiol. 2019;149:49-86. https://doi.org/10.1016/bs.irn.2019.10.013
16. Федорова Н.В., Бриль Е.В., Кулуа Т.К. Прогрессирующий надъядерный паралич: клинические фенотипы. Бюллетень Национального общества по изучению болезни Паркинсона и расстройств движений. 2020;(2):211-214 [Fedorova N.V., Bril' E.V., Kulua T.K. Progressiruyushchii nad"yadernyi paralich: klinicheskie fenotipy. Byulleten' Natsional'nogo obshchestva po izucheniyu bolezni Parkinsona i rasstroistv dvizhenii. 2020;(2):211-214 (In Russ.)]. https://doi.org/10.24412/2226-079X-2022-12470
17. Williams D.R., de Silva R., Paviour D.C. et al. Characteristics of two distinct clinical phenotypes in pathologically proven progressive supranuclear palsy: Richardson's syndrome and PSP-parkinsonism. Brain. 2005;128(Pt 6):1247-58. https://doi.org/10.1093/brain/awh488
18. O'Sullivan S.S., Massey L.A., Williams D.R. et al. Clinical outcomes of progressive supranuclear palsy and multiple system atrophy. Brain. 2008;131(Pt 5):1362-72. https://doi.org/10.1093/brain/awn065
19. Магжанов Р.В., Давлетова А.И., Ибатуллин Р.А. и др. Трудности дифференциальной диагностики прогрессирующего надъядерного паралича и болезни Паркинсона. Анналы клинической и экспериментальной неврологии. 2016;10(4):58-61 [Magzhanov R.V., Davletova A.I., Ibatullin R.A. et al. Trudnosti differentsial'noi diagnostiki progressiruyushchego nad"yadernogo paralicha i bolezni Parkinsona. Annaly klinicheskoi i eksperimental'noi nevrologii. 2016;10(4):58-61 (In Russ.)]. https://doi.org/10.17816/psaic22
20. Захаров В.В., Вахнина Н.В., Гоголева А.Г., Межмидинова С.К. Диагностика и лечение хронической ишемии головного мозга. Медицинский совет. 2020;(8):11-20 [Zakharov V.V., Vakhnina N.V., Gogoleva A.G., Mezhmidinova S.K. Diagnostics and treatment of chronic cerebral ischemia. Meditsinskiy sovet = Medical Council. 2020;(8):36-45 (In Russ.)]. https://doi.org/10.21518/2079-701X-2020-8-36-45
21. Lagarde J., Hamelin L., Hahn V. et al. Progressive Supranuclear Palsy Syndrome and Semantic Dementia in Neuropathologically Proven Lewy Body Disease: A Report of Two Cases. J Alzheimers Dis. 2015;47(1):95-101. https://doi.org/10.3233/JAD-150203
Об авторах
Юрий Николаевич БыковРоссия
д.м.н., профессор, заведующий кафедрой нервных болезней
Елена Игоревна Панферова
Россия
ординатор кафедры нервных болезней
Татьяна Николаевна Загвозкина
Россия
заведующая неврологическим отделением клиник
Юлия Алексеевна Скворцова
Россия
ординатор кафедры нервных болезней
Арина Валерьевна Широкова
Россия
врач-невролог неврологического отделения клиник
Дополнительные файлы
Рецензия
Для цитирования:
Быков Ю.Н., Панферова Е.И., Загвозкина Т.Н., Скворцова Ю.А., Широкова А.В. ДИССОЦИАЦИЯ КЛИНИЧЕСКИХ ПРОЯВЛЕНИЙ И НЕЙРОВИЗУАЛИЗАЦИИ ПРИ ПРОГРЕССИРУЮЩЕМ НАДЪЯДЕРНОМ ПАРАЛИЧЕ (ПАРНОЕ КЛИНИЧЕСКОЕ НАБЛЮДЕНИЕ СИНДРОМА СТИЛА-РИЧАРДСОНА-ОЛЬШЕВСКОГО). Байкальский медицинский журнал. 2025;4(4):83-92. https://doi.org/10.57256/2949-0715-2025-4-4-83-92
For citation:
Bykov Yu., Panferova E., Zagvozkina T., Skvortsova I., Shirokova A. DISSOCIATION OF CLINICAL MANIFESTATIONS AND NEUROIMAGING IN PROGRESSIVE SUPRANUCLEAR PALSY (PAIRED CLINICAL CASE OF STEELE-RICHARDSON-OLSHEVSKY SYNDROME). Baikal Medical Journal. 2025;4(4):83-92. (In Russ.) https://doi.org/10.57256/2949-0715-2025-4-4-83-92
JATS XML
















